La FRANCE est assignée devant la Cour Européenne des justices pour la pollution
recommandation_1432_Conseil_de_l_Europe
petition_changement_d_heure_2015
Cen'est qu'un au revoir -Andre Rieu-Concert-Auld Lang Syne
La subsidiarité vise à répartir les compétences entre l’Union européenne et les États membres en fonction du niveau qui convient le mieux en partant du principe que l’intervention européenne doit être justifiée par le fait que « les objectifs de l’action envisagée ne peuvent pas être atteints de manière suffisante par les États membres ». La nature transfrontière de la pollution de l’air, particulièrement pour l’ozone et les particules, justifie l’action européenne en résonance avec le Traité sur l’Union européenne visant « les dimensions ou les effets de l’action envisagée »
L’intervention du législateur communautaire est néanmoins beaucoup plus ancienne. Une législation spécifique a en effet été mise en place à partir des années 1980 tend à limiter, dans chaque État membre, les concentrations ambiantes de certains polluants identifiés comme néfastes à la santé humaine et à l’environnement : dioxyde de soufre et particules en suspension en 1980, plomb en 1982, dioxyde d’azote en 1985, ozone en 1992. En 1996, une directive-cadre sur l’évaluation et la gestion de la qualité de l’air ambiant a posé les principes de base d’une stratégie commune visant à définir et fixer des objectifs concernant la qualité de l’air ambiant et à évaluer la qualité de l’air ambiant dans les États membres. Pour son application, ont été adoptées des « directives-filles » visant à actualiser les normes édictées pour les polluants déjà réglementés (SO2, NO2,particules, plomb) et à élargir à la réglementation à de nouveaux polluants (benzène, monoxyde de carbone, hydrocarbures aromatiques polycycliques, métaux lourds). La directive-cadre de 1996 et ses directives-filles ont, par souci de simplification, été remplacées par la directive Air pur pour l’Europe à compter du 11 juin 2010 (Directive 2008/50/CE du 21 mai 2008), à l’exception provisoire de la directive 2004/107/CE du 15 décembre 2004 relative aux métaux toxiques et aux HAP dans l’air ambiant. Les valeurs limites de qualité de l’air fixées par le droit de l’Union européenne doivent être respectées par les États membres qui peuvent être lourdement condamnés en cas de manquement.Pollution et qualité de l’air dans l’UE
De nombreux Européens sont extrêmement préoccupés par la pollution de l’air. Celle-ci nuit aux aux voies pulmonaires et respiratoires et peut provoquer de l’asthme, des bronchites et des maladies cardiovasculaires.
Malgré une amélioration générale de la qualité de l’air, la pollution due aux particules fines et à l’ozone troposphérique (ou ozone de basse altitude) continue de provoquer de nombreux décès prématurés chaque année dans l’UE. Elle réduit l’espérance de vie et coûte des milliards d’euros par an en soins de santé.
La pollution atmosphérique a également de nombreux effets néfastes pour l’environnement.
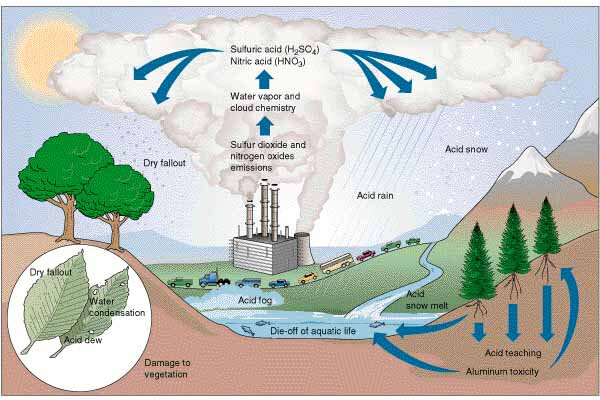
Les polluants tels que le dioxyde de soufre, les oxydes d'azote et l'ammoniac provoquent des pluies acides qui polluent les forêts, les rivières, les lacs et d'autres espaces naturels.
L’eutrophisation est due à la présence de niveaux élevés de nutriments azotés dans la nature. Elle est en grande partie responsable de la diminution de la biodiversité. En s'infiltrant dans les lacs et les cours d'eau, ces nutriments favorisent la prolifération d’algues, qui asphyxient les poissons et d’autres espèces sauvages.
L’ozone troposphérique (ou ozone de basse altitude) endommage le feuillage des végétaux et ralentit leur croissance, porte atteinte aux forêts et aux plantes sauvages et réduit les rendements agricoles.
Les principaux responsables de la pollution atmosphérique sont le secteur de l’énergie, le chauffage domestique, l'industrie lourde (aciéries et raffineries de pétrole), les transports, l’agriculture et le traitement des déchets et le changement d'heure
La législation européenne fixe des normes strictes pour les substances suivantes:
-
Particules: fines particules inférieures à un millimètre de diamètre. Principaux responsables: les transports, la plupart des formes de combustion et certains procédés industriels.
-
Ozone troposphérique (ou ozone de basse altitude): formé par la réaction des oxydes d’azote et des composés organiques volatils en présence de la lumière, ce qui en fait un problème majeur durant l'été.
-
Composés organiques volatils: ils sont émis par les solvants, peintures et vernis, les gaz d'échappement des voitures et les stations-service.
-
Oxydes d’azote, y compris le dioxyde d’azote: ils sont produits durant la combustion (moteurs de véhicules et centrales thermiques, augmentation par l’acide nitreux lors du changement d’heure)
-
Dioxyde de soufre: formé lors de la combustion de combustibles fossiles.
-
Ammoniac (NH3): émis par les déchets animaux et les engrais et les boues des stations d’epurations etendue de Mars a octobre dans les champs)
-
Métaux lourds: ils proviennent de procédés industriels tels que la purification des métaux et la galvanoplastie, l’incinération des déchets et la combustion du charbon dans les centrales électriques (mercure).des boues des stations d'épuration étendue dans les champs de Mars a octobre
-
Benzène: ce solvant industriel largement utilisé est émis à partir de multiples sources: activités industrielles, gaz d’échappement des voitures, stations-service, fumée produite la combustion du bois et cigarettes.
-
Vapeur d’eau des centrales nucléaires
La France est en situation de dépassement des valeurs limites pour les PM10 (figure 1) et pour le NO2 (figure 2). Le montant de l’amende pour le seul contentieux « particules » pourrait s’élever à plus de 100 millions d’euros la première année, puis 90 millions par an les années suivantes, et ce tant que des dépassements seront observés. La Commission européenne a adressé en février 2017 un dernier avertissement à la France pour les dépassements répétés de la valeur limite de NO2 dans 19 zones de qualité de l’air. Le même avertissement a été adressé à l’Allemagne, à l’Espagne, à l’Italie et au Royaume-Uni au motif que ces pays n’ont pas remédié aux infractions répétées aux limites en matière de pollution atmosphérique fixées pour le dioxyde d’azote (NO2).
La France est en situation volontaire de violation du droit européen pour non respect de la recommandation 1432 du Conseil de l’Europe
La france refuse de suivre et respecter le seuil a la protection de la santé sur l’Ozone et n’applique pas les recommandation de lO.M.S sur les seuils de
100µg/M3 d’air sur 8h c’est a dire de 12H à 20h en heure d'été de pétain 1942
Cette mesure horaire évite de faire entrer des heures de nuits qui abaissent naturellement le seuil et artificiellement
La nuit l'ozone, produit à la lumière du jour (grâce au rayonnement du soleil), disparaît.
Le monoxyde d'azote réagit avec l'ozone pour former du dioxyde d'azote.
monoxyde d'azote + ozone -> dioxyde d'azote
10 % de la concentration en ozone dans la troposphère va provenir de la stratosphère en hiver et au printemps. Le reste proviendra des émissions du sol.L'ozone troposphérique va se former à partir de deux types de polluants sous l'action des ultraviolets :
-
la combustion des hydrocarbures sous forme d'oxyde d'azote ;
-
les composés organiques volatiles (COV) issues des solvants, des vapeurs d'essence et certains composés émis par la végétation.
Les pics d'ozone troposphérique seront plus importants au printemps et en été dû aux ultraviolets plus forts combinés aux émissions d'oxyde d'azote et de COV pour former l'ozone.
Les pics d'ozone ne sont jamais très long car ce type de pollution est très mobile. Effectivement, l'ozone formé dans la troposphère peut être transporté à quelques centaines de kilomètres de son lieu de formation grâce au vent. En france la modélisation servant à la surveillance de l’air ne tient pas compte du vent et de sa vitesse
L’ozone est aggravé par le déplacement des activités humaines vis à vis du soleil C’est a dire que la production industrielle,tertiaire et des services sont soumises au pic des UV a 14H jusqu'à 20H ...L'intensité des UV diminue naturellement a partir de 14 jusqu’au coucher du soleil
La vapeur d’eau des centrales nucléaires vont jouer un role aggravant dans la stratosphère sur la molécule d’ozone et du dioxyde d’azote
Toutes les pollutions émises vont être aggravées et augmentées par les UV environ de 30 à 40% par heure pour la journée
La pollution émise à 8H va être soumise au UV et à l’acide nitreux qui vont aggraver et augmenter la photochimie des polluants Ozone,dioxyde d’azote et les COV
Les transports n’ont aucune influence sur ces polluant car il ne représentent que 23% de l'émission
Le facteur heure d'été devient un fléau et une calamité pour le patrimoine naturel et culturel de notre pays
A cela il faudra ajouter le facteur pluies acides Hno3 qui va avoir une influence négatives sur l’utilisation des produits phytosanitaires fongicides et pesticides
Suite a tous ses informations j’ai déposé une plainte à l’encontre de la france pour violation volontaire du droit européen
La france a manipulé l’opinion publique en dénonçant sans cesse les transports comme seul responsable de la pollution atmosphérique
Mais en aout 2003 et Août 2015 les français seront en vacances et la pollution était responsable des 30.000 morts et des 6000 morts en 2015 par ce laxisme volontaire
Le Secretaire General au Ministere de l’Environnement est complice de ce crime en 2015 et 20O3
Le collabo Maurice Papon secrétaire Général de la préfecture de la Gironde fut condamné pour complicité de crime contre l’Humanité
Absorption du rayonnement UV : réactions photochimiques
Dans le cas de l’ozone, l’énergie requise pour la dissociation d’une liaison covalente entre deux atomes d’oxygène est de l’ordre de 100 kJ.mol-1. Cela correspond à un rayonnement de longueur d’onde 1180 nm qui se situe dans l’infrarouge. En pratique, l’absorption est observée dès que la longueur d’onde des photons incidents sur l’ozone est inférieure à 1180 nm ce qui déclenche la réaction de dissociation suivante :
(1) O3 + photon → O2 + O
Le rayonnement UV étant de longueur d’onde inférieure à 400 nm, il possède une énergie largement suffisante pour provoquer photodissociation de l’ozone. Il faut signaler que dans le cas d’une longueur d’onde inférieure à 310 nm, la photodissociation libère un atome d’oxygène excité, c’est à dire porté à une énergie supérieure à son énergie minimale. Un tel atome est noté O* et on écrit la réaction de dissociation de deux façons différentes suivant la longueur d’onde absorbée :
(2) O3 + photon → O2 + O si 310 ≤ λ ≤ 1180 nm
(3) O3 + photon → O2 + O si λ ≤ 310 nm
La photodissociation (2) est responsable de l’absorption d’une partie des UV-A et la réaction (3) explique l’absorption de la quasi-totalité des UV-B dans la stratosphère. Les UV-C sont totalement absorbés selon (3) entre 242 à 280 nm et pour les longueurs d’onde inférieure à 242 nm on observe également la réaction de photodissociation du dioxygène (4) dont la contribution à l’absorption des UV-C devient déterminante :
(4) O2 + photon → 2 O si λ ≤ 242 nm
On peut signaler que ce sont les atomes d’oxygène ainsi formés qui vont permettre la formation de l’ozone stratosphérique par réaction sur le dioxygène (5) :
(5) O2 + O → O3
Enfin, ces atomes d’oxygène peuvent également réagir sur l’ozone pour former du dioxygène selon (6) :
(6) O3 + O → 2 O2
L’ozone est donc au coeur d’un équilibre dynamique au sein duquel il est continuellement créé et détruit. C’est le cycle de Chapman [3] dont le bilan est l’équilibre (7) :
(7) 3 O2 → 2 O3
Influence de l’ozone sur la température de l’atmosphère
Pour comprendre l’influence de l’ozone stratosphérique sur la température de l’atmosphère, il faut examiner plus en détail la réaction (5) de formation de l’ozone. Pour former l’ozone à partir du dioxygène, il faut former une liaison O-O, or la formation de liaison est une réaction exothermique : elle libère de l’énergie dans le milieu. Cette énergie est égale à l’énergie de la liaison créée (on note la symétrie par rapport à la réaction de dissociation qui nécessite elle d’apporter au moins l’énergie de la liaison pour la briser.)
Pour que la dissociation soit complète, l’énergie libérée doit impérativement être récupérée par une troisième entité également engagée dans le choc. En effet, dans le cas contraire, l’énergie est immédiatement réutilisée pour briser la liaison à peine formée, on parle alors d’un choc non-réactif (réaction 8). La troisième entité est appelée « auxiliaire de choc ». Elle peut être n’importe quelle espèce du milieu, en l’occurrence c’est une des espèces les plus abondantes dans l’atmosphère : N2 ou O2, nous la noterons M. La réaction de formation de l’ozone s’écrit donc (9) :
(8) O2 + O → O3 → O2 + O
(9) O2 + O + M → O3 + M*
Il apparaît donc une espèce M* excitée lors d’un choc réactif. Celle-ci se désexcite rapidement au cours de chocs avec les autres constituants de l’atmosphère durant lesquels elle leur transfère une partie de son énergie sous forme d’énergie cinétique. Cette augmentation de l’agitation moléculaire se traduit par un échauffement du milieu








/https%3A%2F%2Fstorage.canalblog.com%2F45%2F32%2F1390704%2F133521916_o.jpg)
/http%3A%2F%2Fstorage.canalblog.com%2F49%2F49%2F1390704%2F132600320_o.jpg)
/http%3A%2F%2Fstorage.canalblog.com%2F46%2F89%2F1390704%2F125594904_o.jpg)
/http%3A%2F%2Fstorage.canalblog.com%2F14%2F19%2F1390704%2F127848585_o.png)